当超声波与介质或生物体相互作用时,除了能够形成空化和温升等效应外,还会产生可用于远程操控的声辐射力。利用这一物理现象,可望实现从无创神经调控到功能微粒的精准操控。然而,要将相关基础研究切实应用于临床复杂场景,目前仍面临巨大的挑战。例如,在血流、颅骨及运动器官等多变且高衰减的生理环境中,如何实现高精度的声场时空分布控制,需要研制针对不同应用需求的专用发射器件,并开发优化的空间声学计算算法来精确模拟与调控声能量分布。
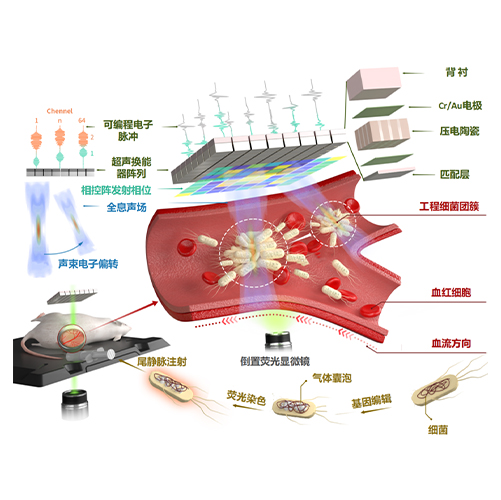
在神经调控方面,若要通过超声穿过颅骨并将安全、有效剂量及特定形状的声场聚焦到大脑深部区域,实现精准的深部脑刺激,就必须设计专门的声辐射力换能器并研发特殊的超声穿颅发射算法,以在有限空间内实现最大化的聚焦效率与安全性。而在声操控领域,相较于获得诺贝尔物理学奖的光镊,声镊具有更强的作用力、更大的组织穿透深度以及不需要荧光标记等优势,因而在细胞治疗和组织工程中拥有广阔的应用前景。然而,由于生物体内部环境极其复杂,声镊在真实生物系统中的应用研究仍处于起步阶段,尚需在器件设计、声场计算与全息成像等方面开展深入攻关,才能最终实现对细胞、微粒乃至完整组织的稳定操控与精确调控。
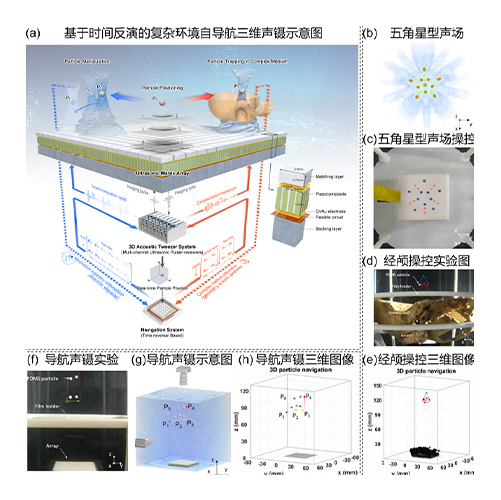
项目团队开展了复杂环境自导航三维声镊研究;首先,将超声B模式成像与三维声镊技术相结合,利用同一个256阵元换能器阵列交替发射成像和操控脉冲序列,实现对操控过程的超声图像实时监测,并利用图像的定位信息反馈,进一步主动引导声镊系统在介质中创建操控声场,完成捕获并移动粒子。此方法可以实现在非透明介质中的声操控。其次,通过将声镊技术与时间反演方法相结合,来矫正声波在非均匀介质中的相位和幅度畸变,从而实现了在复杂环境中的三维粒子操控。如该研究实现了跨越离体人类头骨操控PDMS粒子沿着特定三维轨迹运动。
相关研究成果已经发表在综合类顶级期刊Research上,对本项目中拟开展的复杂介质中的三维全息声操控方法研究具有重要的指导意义。
(a)基于时间反演的复杂环境自导航三维声镊示意图。
(b)10个焦点排列成五角星形的仿真三维声场图。
(c)利用10个焦点声场操控PDMS粒子。
(d)经过人类颅骨操控粒子运动过程的三维超声图像。
(e)经过人类颅骨操控PDMS粒子实验的侧视图。
(f) 基于时间反演的复杂环境自导航三维声镊操控粒子运动实验图。
(g) 基于时间反演的复杂环境自导航三维声镊操控粒子运动实验示意图。
(h) 基于时间反演的复杂环境自导航三维声镊操控粒子运动过程的三维超声图像。
相关研究成果已经发表在综合类顶级期刊Research上,对本项目中拟开展的复杂介质中的三维全息声操控方法研究具有重要的指导意义。
(a)基于时间反演的复杂环境自导航三维声镊示意图。
(b)10个焦点排列成五角星形的仿真三维声场图。
(c)利用10个焦点声场操控PDMS粒子。
(d)经过人类颅骨操控粒子运动过程的三维超声图像。
(e)经过人类颅骨操控PDMS粒子实验的侧视图。
(f) 基于时间反演的复杂环境自导航三维声镊操控粒子运动实验图。
(g) 基于时间反演的复杂环境自导航三维声镊操控粒子运动实验示意图。
(h) 基于时间反演的复杂环境自导航三维声镊操控粒子运动过程的三维超声图像。